नई दिल्ली, 9 अक्टूबर (पीटीआई) — विश्व स्वास्थ्य संगठन (WHO) ने गुरुवार को भारतीय अधिकारियों से यह जानने की कोशिश की है कि देश में बच्चों की मौतों से जुड़ी खांसी की सिरप क्या अन्य देशों में निर्यात की गई थी, सूत्रों ने बताया।
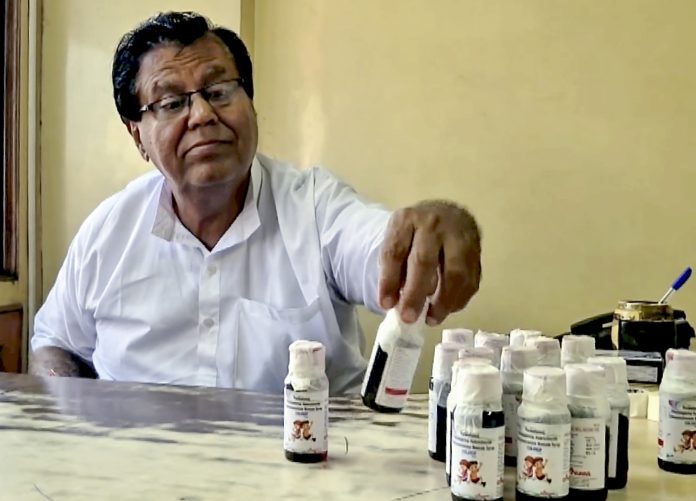
सूत्रों के अनुसार, वैश्विक स्वास्थ्य एजेंसी अधिकारियों से आधिकारिक पुष्टि मिलने के बाद खांसी की सिरप, कोल्डरिफ (Coldrif) पर ‘ग्लोबल मेडिकल प्रोडक्ट अलर्ट’ जारी करने का निर्णय लेगी। एजेंसी ऐसी अलर्ट्स उप-मानक और दूषित दवाओं के लिए जारी करती है।
मध्य प्रदेश के पांच बच्चे गंभीर स्थिति में हैं, जबकि 20 बच्चों की मौत “दूषित” खांसी की सिरप के सेवन से हुई, जिसमें डाइएथिलीन ग्लाइकोल (DEG) और एथिलीन ग्लाइकोल (EG) शामिल थे।
इसके अलावा, राजस्थान के विभिन्न जिलों में कम से कम तीन बच्चों की खांसी की सिरप पीने के बाद मौत होने की खबरें मिली हैं।
सूत्रों ने कहा, “विश्व स्वास्थ्य संगठन (WHO) ने बुधवार को यह स्पष्ट करने के लिए कहा है कि क्या देश में बच्चों की मौतों से जुड़ी खांसी की सिरप अन्य देशों में निर्यात की गई थी, जो कि नियमित प्रक्रिया का हिस्सा है।”
भारत के ड्रग्स कंट्रोलर जनरल (DCGI) ने बुधवार को सभी राज्य और केंद्र शासित प्रदेशों के ड्रग नियंत्रकों से कहा कि वे फार्मास्यूटिकल उत्पादों के कच्चे माल और तैयार फार्मूलेशनों का परीक्षण सुनिश्चित करें, खासकर मध्य प्रदेश में बच्चों की मौत के संदिग्ध मामले के बाद।
DCGI ने अपने परामर्श में कहा कि हाल की निरीक्षण रिपोर्टों और ‘नियमों के अनुरूप नहीं’ घोषित दवाओं की जांच के दौरान यह पाया गया कि कई निर्माता उपयोग से पहले प्रत्येक बैच के सहायक तत्वों और सक्रिय अवयवों का परीक्षण नहीं कर रहे हैं।
परामर्श में कहा गया, “निर्माण सुविधाओं में किए गए निरीक्षणों और ‘Not of Standard Quality’ घोषित दवाओं की जांच में पाया गया कि निर्माता प्रत्येक बैच के सहायक/सक्रिय दवा अवयवों का परीक्षण निर्धारित मानकों के अनुरूप नहीं कर रहे हैं। इसे सुनिश्चित करना होगा कि ये परीक्षण निर्माण और बाजार में रिलीज़ से पहले किए जाएँ।”
DCGI ने सभी राज्य/केन्द्र शासित प्रदेशों के ड्रग नियंत्रकों से अनुरोध किया कि वे निरीक्षणों, परिपत्रों आदि के माध्यम से निर्माता को जागरूक करें और यह सुनिश्चित करें कि निर्माता केवल विश्वसनीय अनुमोदित विक्रेताओं से कच्चा माल और सहायक तत्व इस्तेमाल करें।
केंद्र ने 2023 में फार्मा कंपनियों को निर्देश दिया था कि खुराक संयोजन (FDC) क्लोरफेनिरामिन मेलिएट IP 2mg और फिनाइलएफ्रीन HCl IP 5mg ड्रॉप/मिलीलीटर के लेबल और पैकेज में चेतावनी अंकित करें कि “चार वर्ष से कम उम्र के बच्चों में इसका उपयोग नहीं करना चाहिए।”
(पीटीआई)
श्रेणी: ब्रेकिंग न्यूज़
एसईओ टैग्स: #स्वदेशी, #समाचार, बच्चों की मौतों से जुड़ी खांसी की सिरप क्या अन्य देशों में भेजी गई: WHO ने भारतीय अधिकारियों से पूछा
